Qu'est-ce que Keytruda - Pembrolizumab et dans quel cas est-il utilisé ?
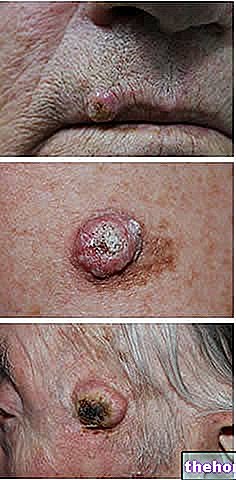
Keytruda est un médicament anticancéreux utilisé pour traiter les adultes atteints d'un mélanome (un type de cancer de la peau) qui s'est propagé à d'autres parties du corps ou qui ne peut être retiré par chirurgie.
Keytruda contient le principe actif pembrolizumab
Comment Keytruda est-il utilisé - Pembrolizumab ?
Le traitement par Keytruda doit être instauré et supervisé par un médecin spécialiste expérimenté dans l'utilisation des médicaments anticancéreux.Le médicament n'est délivré que sur ordonnance.
Keytruda est disponible sous forme de poudre à reconstituer en solution pour perfusion (goutte-à-goutte dans une veine). La perfusion est administrée à la dose recommandée de 2 mg par kilogramme de poids corporel pendant 30 minutes toutes les trois semaines. En cas de certains effets indésirables, le médecin peut décider de reporter l'administration des doses ou, selon la gravité des effets, d'interrompre le traitement. Le traitement doit se poursuivre jusqu'à ce que la maladie s'aggrave ou que des effets secondaires ingérables apparaissent.
Pour plus d'informations, consultez la notice.
Comment Keytruda - Pembrolizumab agit-il ?
Le principe actif de Keytruda, le pembrolizumab, est un anticorps monoclonal. Un anticorps monoclonal est un anticorps (un type de protéine) conçu pour reconnaître et se fixer à une structure spécifique, appelée antigène, présente dans certaines cellules du corps.
Le pembrolizumab a été conçu pour se fixer et bloquer un récepteur appelé « mort cellulaire programmée 1 » (PD-1), qui annule l'activité de certaines cellules du système immunitaire (les défenses naturelles de l'organisme) appelées « cellules T ». En bloquant PD-1, le pembrolizumab empêche ce récepteur d'inhiber ces cellules immunitaires, augmentant ainsi la capacité du système immunitaire à détruire les cellules de mélanome.
Quel bénéfice Keytruda - Pembrolizumab a-t-il montré au cours des études ?
Keytruda s'est avéré efficace dans le traitement des patients atteints d'un mélanome inopérable ou s'est propagé dans tout le corps dans deux études principales.
La première étude a inclus 540 patients qui avaient été précédemment traités avec un autre anticorps monoclonal utilisé dans le traitement du mélanome, l'ipilimumab. Les patients ont été traités par Keytruda à une dose de 2 mg/kg de poids corporel toutes les trois semaines ou à une dose de 10 mg/kg de poids corporel toutes les trois semaines ou par chimiothérapie (médicaments utilisés dans le traitement du cancer). Les premiers résultats ont montré que, 6 mois après le début du traitement, la maladie ne s'était pas aggravée chez 34 % des patients traités par Keytruda contre 16 % des patients traités par chimiothérapie.
La deuxième étude a porté sur 834 patients n'ayant jamais été traités par ipilimumab et ayant reçu soit Keytruda, soit ipilimumab. Les premiers résultats ont montré que les patients traités par Keytruda ont survécu jusqu'à 5,5 mois sans progression de la maladie contre 2,8 mois pour les patients traités par ipilimumab. L'étude a également révélé que la survie globale était plus élevée chez les sujets traités par Keytruda que chez les patients traités par ipilimumab. Jusqu'à 71 % des patients ont survécu au moins 12 mois après le début du traitement, contre 58 % des sujets traités par ipilimumab.
Quel est le risque associé à Keytruda - Pembrolizumab ?
Les effets indésirables les plus fréquents avec Keytruda (pouvant affecter plus d'1 personne sur 10) sont la diarrhée, les nausées, les démangeaisons, l'érythème, l'arthralgie (douleurs articulaires) et la fatigue, qui sont pour la plupart d'intensité légère à modérée. Autres effets indésirables fréquents avec Keytruda liés à l'activité du système immunitaire, qui est responsable de l'inflammation des organes.La plupart des effets indésirables disparaissent avec un traitement adéquat ou lorsque le traitement avec Keytruda est arrêté.
Pour la liste complète des effets indésirables rapportés avec Keytruda et leurs restrictions, voir la notice.
Pourquoi Keytruda - Pembrolizumab a-t-il été approuvé ?
Le comité des médicaments à usage humain (CHMP) de l'Agence a décidé que les bénéfices de Keytruda sont supérieurs à ses risques et a recommandé que son utilisation soit approuvée dans l'UE.Le CHMP a pris en compte que les résultats des études disponibles, bien que non définitifs, ont révélé les bénéfices de Keytruda chez les sujets atteints de mélanome avancé.Le profil de tolérance a été jugé favorable par rapport aux autres traitements, dont l'ipilimumab et la chimiothérapie, et les effets secondaires sont gérables avec les recommandations existantes.
Quelles mesures sont prises pour garantir l'utilisation sûre et efficace de Keytruda - Pembrolizumab ?
Un plan de gestion des risques a été élaboré pour garantir que Keytruda est utilisé de la manière la plus sûre possible. Sur la base de ce plan, des informations de sécurité ont été ajoutées au résumé des caractéristiques du produit et à la notice de Keytruda, y compris les précautions appropriées à suivre par les professionnels de santé et les patients.
En outre, la société qui fabrique Keytruda fournira aux médecins qui prescrivent le médicament du matériel éducatif contenant des informations sur l'utilisation de Keytruda et la gestion des effets secondaires, en particulier ceux liés à l'activité du système immunitaire. La société fournira également une carte d'alerte patient avec des informations sur les risques du médicament et quand contacter un médecin si des symptômes apparaissent.
La société mettra également à disposition les résultats finaux des études en cours avec Keytruda pour confirmer les bénéfices à long terme du médicament. Enfin, la société évaluera davantage les doses de 2 mg/kg et 10 mg/kg de poids corporel chez des patients spécifiques et réalisera des tests pour mieux comprendre quels individus peuvent bénéficier le plus du traitement par Keytruda.
Autres informations sur Keytruda - Pembrolizumab
Le 17 juillet 2015, la Commission européenne a délivré une « autorisation de mise sur le marché » pour Keytruda, valable dans toute l'Union européenne.
Pour plus d'informations sur le traitement par Keytruda, veuillez lire la notice (incluse dans l'EPAR) ou contacter votre médecin ou votre pharmacien.
Dernière mise à jour de ce résumé : 07-2015.
Les informations sur Keytruda - Pembrolizumab publiées sur cette page peuvent être obsolètes ou incomplètes. Pour une utilisation correcte de ces informations, consultez la page Avis de non-responsabilité et informations utiles.